秘魯醫療器械注冊

秘魯醫療器械監管流程基于第29459號法律(藥品、醫療器械和健康產品法)和第016-2013-SA號最高法令(藥品、醫療器械和健康產品注冊、控制和健康監督條例)及其修正案。秘魯的醫療器械還適用其他一些法規。

在秘魯,負責醫療器械監管的機構是 Dirección General de Medicamentos,Insumos y Drogas(DIGEMID)。
該機構隸屬于衛生部(Ministerio de Salud或MINSA
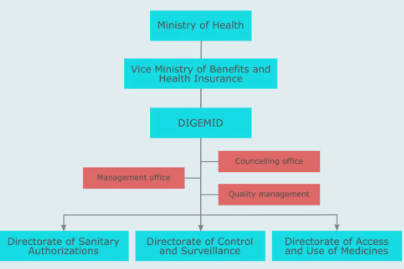
衛生授權局負責決定秘魯醫療器械的注冊和拒絕。一般而言,衛生授權局負責:
醫療器械注冊
恢復
修改
拒絕
暫停
根據國家醫療器械法規,取消藥品、醫療器械和衛生產品的衛生注冊或衛生證書。
秘魯的醫療器械根據其相關風險分為四類:
I類-低風險醫療器械
II類-中等風險醫療器械
第三類-高風險醫療器械
第四類-危險醫療器械
通過 RegDesk 警報,您可以隨時跟蹤變化,我們會在秘魯監管部門發生變化時發出警告。
產品注冊:
秘魯所有醫療設備必須在DIGEMID注冊,以便制造商能夠在秘魯銷售。注冊過程平均需要4到5個月,盡管準確的長度在很大程度上取決于設備的分類。風險較低的醫療器械通常審批速度較快,而風險較高的器械審批時間較長。
Class I - 60 days
Class II - 90 days
Classes III, IV - 120 days
注冊申請一經批準,注冊證書有效期為5年。如果制造商打算在這段時間后繼續在秘魯銷售他們的設備,他們必須提交續期申請。
對于總部位于秘魯境外的制造商,還需要指定授權代表或秘魯注冊持有人(PRH),以便向DIGEMID成功注冊設備。
PRH負責醫療器械注冊,并且必須在其負責的器械標簽上注明。
在秘魯申請注冊的設備制造商必須提供以下信息:
有關設備及其組件的詳細信息
包裝和標簽信息
設備的所有測試結果
自由銷售證書(CFS)或外國政府證書(CFG)(如適用)
在緊急情況下,可以在一種情況下使用、進口和/或制造未經官方營銷授權的醫療器械。在這種情況下,DIGEMID必須給予制造商批準才能這樣做。當迫切需要某一特定設備用于研究和培訓目的或用于嚴重預防和個體治療時,就會出現這種情況。
秘魯最新監管事務更新
2017年6月5日,DIGEMID發布了一項法令(文件以西班牙語書寫),其中包括以下變更:
簡化了制造商獲取進口證書的要求。
現在需要中高風險醫療器械的風險管理報告。
所有醫療器械類別的官方審查時間已縮短30天。
如您有相關產品需要咨詢,歡迎您直接來電4000-1998-38咨詢我司工作人員,獲得詳細的費用報價與周期方案等信息。



